Tốc độ ăn mòn là một thông số đa yếu tố phụ thuộc cả vào điều kiện môi trường bên ngoài và các đặc tính bên trong của vật liệu. Trong tài liệu quy chuẩn và kỹ thuật, có những hạn chế nhất định về giá trị cho phép của sự phá hủy kim loại trong quá trình vận hành của thiết bị và kết cấu công trình để đảm bảo chúng hoạt động không gặp sự cố. Trong kỹ thuật, không có phương pháp chung nào để xác định tốc độ ăn mòn. Điều này là do sự phức tạp của việc tính đến tất cả các yếu tố. Phương pháp đáng tin cậy nhất là nghiên cứu lịch sử hoạt động của cơ sở.
Tiêu chí

Hiện tại, một số tốc độ ăn mòn được sử dụng trong thiết kế kỹ thuật:
- Theo phương pháp đánh giá trực tiếp: giảm khối lượng của một chi tiết kim loại trên một đơn vị bề mặt - chỉ thị khối lượng (đo bằng gam trên 1 m2trong 1 giờ); độ sâu hư hỏng (hoặc độ thấm quá trình ăn mòn), mm / năm; lượng của pha khí thoát ra của các sản phẩm ăn mòn; khoảng thời gian mà hư hỏng ăn mòn đầu tiên xuất hiện; số lượng tâm ăn mòn trên một đơn vị diện tíchbề mặt xuất hiện trong một khoảng thời gian nhất định.
- Ước tính gián tiếp: cường độ dòng điện ăn mòn điện hóa; điện trở; thay đổi các đặc tính vật lý và cơ học.
Chỉ số định giá trực tiếp đầu tiên là phổ biến nhất.
Công thức tính
Trong trường hợp chung, khối lượng giảm xác định tốc độ ăn mòn của kim loại được tìm thấy theo công thức sau:
Vkp=q / (St), trong đó q là sự giảm khối lượng của kim loại, g;
S - diện tích bề mặt mà vật liệu được chuyển từ đó, m2;
t - khoảng thời gian, giờ
Đối với kim loại tấm và vỏ được làm từ nó, hãy xác định chỉ số độ sâu (mm / năm):
H=m / t, m là độ sâu xuyên thấu vào kim loại.
Có mối quan hệ sau giữa chỉ số thứ nhất và thứ hai được mô tả ở trên:
H=8, 76Vkp/ ρ, trong đó ρ là mật độ của vật liệu.
Các yếu tố chính ảnh hưởng đến tốc độ ăn mòn
Các nhóm yếu tố sau ảnh hưởng đến tốc độ phá hủy kim loại:
- bên trong, liên quan đến bản chất vật lý và hóa học của vật liệu (cấu trúc pha, thành phần hóa học, độ nhám bề mặt của bộ phận, ứng suất dư và vận hành trong vật liệu, và những thứ khác);
- bên ngoài (điều kiện môi trường, tốc độ di chuyển của môi trường ăn mòn, nhiệt độ, thành phần của khí quyển, sự hiện diện của chất ức chế hoặc chất kích thích, và những thứ khác);
- cơ học (phát triển các vết nứt do ăn mòn, phá hủy kim loại dưới tác dụng của tải trọng theo chu kỳ,sự xâm thực và sự ăn mòn khó chịu);
- tính năng thiết kế (lựa chọn loại kim loại, khoảng cách giữa các bộ phận, yêu cầu về độ nhám).
Tính chất vật lý và hóa học
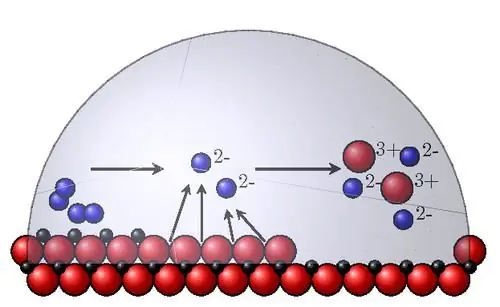
Các yếu tố ăn mòn bên trong quan trọng nhất là:
- Ổn định nhiệt động. Để xác định nó trong dung dịch nước, biểu đồ Pourbaix tham chiếu được sử dụng, dọc theo trục abscissa trong đó pH của môi trường được vẽ và dọc theo trục tọa độ, điện thế oxy hóa khử. Một sự thay đổi tiềm năng theo hướng tích cực có nghĩa là vật liệu có độ ổn định cao hơn. Theo dự kiến, nó được định nghĩa là thế cân bằng thông thường của kim loại. Trong thực tế, vật liệu bị ăn mòn ở các tốc độ khác nhau.
- Vị trí của nguyên tử trong bảng tuần hoàn các nguyên tố hóa học. Kim loại dễ bị ăn mòn nhất là kim loại kiềm và kim loại kiềm thổ. Tốc độ ăn mòn giảm khi số nguyên tử tăng lên.
- Cấu trúc tinh thể. Nó có một tác dụng không rõ ràng đối với sự phá hủy. Bản thân cấu trúc hạt thô không dẫn đến sự gia tăng ăn mòn, nhưng thuận lợi cho sự phát triển của sự phá hủy có chọn lọc giữa các hạt của các ranh giới hạt. Kim loại và hợp kim có sự phân bố đồng nhất của các pha ăn mòn đồng đều, trong khi những kim loại có sự phân bố không đồng đều sẽ ăn mòn theo cơ chế tiêu điểm. Sự sắp xếp lẫn nhau của các pha thực hiện chức năng của cực dương và cực âm trong môi trường xâm thực.
- Năng lượng không đồng nhất của các nguyên tử trong mạng tinh thể. Nguyên tử có năng lượng cao nhất nằm ở các góc của mặtmicroroughnesses và là trung tâm hoạt động của sự hòa tan trong quá trình ăn mòn hóa học. Do đó, việc gia công cẩn thận các chi tiết kim loại (mài, đánh bóng, hoàn thiện) làm tăng khả năng chống ăn mòn. Hiệu ứng này cũng được giải thích là do sự hình thành các màng oxit dày đặc hơn và liên tục hơn trên bề mặt nhẵn.
Ảnh hưởng của độ chua trung bình

Trong quá trình ăn mòn hóa học, nồng độ của các ion hydro ảnh hưởng đến các điểm sau:
- khả năng hòa tan của các sản phẩm ăn mòn;
- hình thành màng oxit bảo vệ;
- tốc độ phá hủy kim loại.
Khi pH nằm trong khoảng 4-10 đơn vị (dung dịch axit), sự ăn mòn của sắt phụ thuộc vào cường độ xâm nhập của oxy vào bề mặt của vật thể. Trong dung dịch kiềm, tốc độ ăn mòn đầu tiên giảm do sự thụ động bề mặt, sau đó, ở pH >13, tăng do sự hòa tan của màng oxit bảo vệ.
Đối với mỗi loại kim loại có sự phụ thuộc riêng của cường độ phá hủy vào tính axit của dung dịch. Kim loại quý (Pt, Ag, Au) có khả năng chống ăn mòn trong môi trường axit. Zn, Al bị phá hủy nhanh chóng trong cả axit và kiềm. Ni và Cd có khả năng chống kiềm nhưng dễ bị ăn mòn trong axit.
Thành phần và nồng độ của dung dịch trung tính

Tốc độ ăn mòn trong dung dịch trung tính phụ thuộc nhiều hơn vào tính chất của muối và nồng độ của nó:
- Trong quá trình thủy phân các muối trongtrong môi trường ăn mòn, các ion được hình thành hoạt động như chất hoạt hóa hoặc chất làm chậm (chất ức chế) phá hủy kim loại.
- Những hợp chất làm tăng độ pH cũng làm tăng tốc độ của quá trình phá hủy (ví dụ, tro soda), và những hợp chất làm giảm độ axit làm giảm nó (amoni clorua).
- Khi có clorua và sunfat trong dung dịch, sự phá hủy được kích hoạt cho đến khi đạt được nồng độ muối nhất định (được giải thích là do quá trình cực dương tăng cường dưới ảnh hưởng của các ion clorua và lưu huỳnh), và sau đó giảm dần do độ tan của oxy giảm.
Một số loại muối có khả năng tạo màng không hòa tan (ví dụ: photphat sắt). Điều này giúp bảo vệ kim loại khỏi bị phá hủy thêm. Tính chất này được sử dụng khi sử dụng chất trung hòa rỉ sét.
Chất ức chế ăn mòn
Chất ức chế ăn mòn (hoặc chất ức chế) khác nhau về cơ chế hoạt động của chúng đối với quá trình oxy hóa khử:
- Cực dương. Nhờ chúng, một bộ phim thụ động được hình thành. Nhóm này bao gồm các hợp chất dựa trên cromat và bichromat, nitrat và nitrit. Loại chất ức chế cuối cùng được sử dụng để bảo vệ liên kết các bộ phận. Khi sử dụng chất ức chế ăn mòn anốt, trước tiên cần xác định nồng độ bảo vệ tối thiểu của chúng, vì thêm một lượng nhỏ có thể dẫn đến tăng tốc độ phá hủy.
- Cực âm. Cơ chế hoạt động của chúng dựa trên sự giảm nồng độ oxy và do đó, làm chậm quá trình catốt.
- Che chắn. Các chất ức chế này cô lập bề mặt kim loại bằng cách tạo thành các hợp chất không hòa tan được lắng đọng như một lớp bảo vệ.
Nhóm cuối cùng bao gồm chất trung hòa rỉ sét, cũng được sử dụng để làm sạch ôxít. Chúng thường chứa axit photphoric. Dưới ảnh hưởng của nó, quá trình phốt phát hóa kim loại xảy ra - sự hình thành một lớp bảo vệ mạnh mẽ của phốt phát không hòa tan. Chất trung hòa được sử dụng bằng súng phun hoặc con lăn. Sau 25-30 phút, bề mặt có màu xám trắng. Sau khi chế phẩm khô, sơn và vecni sẽ được áp dụng.
Động cơ

Sự gia tăng ăn mòn trong môi trường xâm thực được tạo điều kiện bởi các loại tác động cơ học như:
- Ứng suất bên trong (trong quá trình đúc hoặc xử lý nhiệt) và bên ngoài (dưới tác động của tải trọng bên ngoài). Kết quả là, sự không đồng nhất điện hóa xảy ra, độ ổn định nhiệt động của vật liệu giảm, và hình thành vết nứt do ăn mòn. Đặc biệt nhanh là sự phá hủy dưới tải trọng kéo (các vết nứt được hình thành trong các mặt phẳng vuông góc) khi có mặt các anion oxy hóa, ví dụ, NaCl. Một ví dụ điển hình về các thiết bị chịu kiểu phá hủy này là các bộ phận của nồi hơi.
- Tác động động, rung động xen kẽ (mòn mỏi). Giới hạn mỏi giảm đi nhiều, nhiều vết nứt nhỏ được hình thành, sau đó hợp nhất thành một vết nứt lớn. Con sốchu kỳ đến mức độ lớn hơn phụ thuộc vào thành phần hóa học và pha của kim loại và hợp kim. Trục bơm, lò xo, cánh tua bin và các thiết bị khác có thể bị ăn mòn.
- Ma sát của các bộ phận. Sự ăn mòn nhanh chóng là do sự mài mòn cơ học của các lớp màng bảo vệ trên bề mặt của chi tiết và tương tác hóa học với môi trường. Trong chất lỏng, tốc độ phá hủy thấp hơn trong không khí.
- Tác động của khoang. Sự tạo khoang xảy ra khi tính liên tục của dòng chất lỏng bị vi phạm do sự hình thành các bong bóng chân không xẹp xuống và tạo ra hiệu ứng dao động. Kết quả là, thiệt hại sâu sắc có tính chất cục bộ xảy ra. Loại ăn mòn này thường thấy trong các thiết bị hóa học.
Yếu tố thiết kế

Khi thiết kế các phần tử hoạt động trong điều kiện khắc nghiệt, phải tính đến tốc độ ăn mòn tăng lên trong các trường hợp sau:
- khi các kim loại khác nhau tiếp xúc với nhau (sự khác biệt về thế điện cực giữa chúng càng lớn thì cường độ dòng điện của quá trình điện hóa bị phá hủy càng cao);
- với sự hiện diện của bộ tập trung ứng suất cơ học (rãnh, rãnh, lỗ, và những thứ khác);
- với độ sạch của bề mặt được gia công thấp, vì điều này dẫn đến các cặp điện bị đoản mạch cục bộ;
- với sự khác biệt đáng kể về nhiệt độ của các bộ phận riêng lẻ của thiết bị (các tế bào điện hóa nhiệt được hình thành);
- với sự hiện diện của các khu vực đọng (khe, khoảng trống);
- khi hình thànhứng suất dư, đặc biệt trong các mối hàn (để loại bỏ chúng, cần phải xử lý nhiệt - ủ).
Phương pháp đánh giá

Có một số cách để đánh giá tốc độ phá hủy kim loại trong môi trường xâm thực:
- Phòng thí nghiệm - thử nghiệm các mẫu trong điều kiện giả lập gần với thực tế. Ưu điểm của họ là cho phép bạn giảm thời gian nghiên cứu.
- Lĩnh vực - được tổ chức trong điều kiện tự nhiên. Họ mất nhiều thời gian. Ưu điểm của phương pháp này là thu được thông tin về các đặc tính của kim loại trong các điều kiện hoạt động tiếp theo.
- Thử nghiệm tại chỗ các vật thể kim loại đã hoàn thiện trong môi trường tự nhiên.






