Khí, theo quan điểm của nhiệt động lực học, được mô tả bằng một tập hợp các đặc tính vĩ mô, trong đó chính là nhiệt độ, áp suất và thể tích. Sự không đổi của một trong các thông số này và sự thay đổi của hai thông số kia cho thấy rằng một hoặc một quá trình đẳng tích khác xảy ra trong khí. Chúng tôi sẽ dành bài viết này để trả lời chi tiết cho các câu hỏi rằng đây là một quá trình đẳng tích, nó khác với sự thay đổi đẳng nhiệt và đẳng áp trong các trạng thái của một hệ khí như thế nào.
Khí lý tưởng trong vật lý

Trước khi trả lời câu hỏi rằng đây là một quá trình đẳng tích, bạn nên hiểu rõ hơn về khái niệm khí lý tưởng. Trong vật lý, nó được hiểu là bất kỳ chất khí nào trong đó động năng trung bình của các hạt cấu thành của nó vượt xa thế năng tương tác của chúng và khoảng cách giữa các hạt này lớn hơn vài bậc so với kích thước tuyến tính của chúng. Trong các điều kiện đã lưu ý, có thể, khi tiến hànhcác phép tính không tính đến năng lượng tương tác giữa các hạt (nó bằng không), và cũng có thể giả định rằng các hạt là các điểm vật chất có khối lượng m nhất định.
Quá trình duy nhất diễn ra trong khí lý tưởng là sự va chạm của các hạt với thành bình chứa chất đó. Những va chạm này biểu hiện trong thực tế là sự tồn tại của một áp suất nhất định trong chất khí P.
Theo quy luật, bất kỳ chất khí nào bao gồm các phân tử tương đối trơ về mặt hóa học và có áp suất thấp và nhiệt độ cao đều có thể được coi là khí lý tưởng với đủ độ chính xác cho các tính toán thực tế.
Phương trình mô tả khí lý tưởng
Tất nhiên, chúng ta đang nói về quy luật phổ quát của Clapeyron-Mendeleev, cần được hiểu rõ để hiểu rằng đây là một quá trình đẳng tích. Vì vậy, phương trình trạng thái phổ quát có dạng sau:
PV=nRT.
Tức là tích của áp suất P và thể tích khí V bằng tích của nhiệt độ tuyệt đối T và lượng chất theo số mol n, trong đó R là hệ số tỉ lệ. Bản thân phương trình lần đầu tiên được viết ra bởi Emile Clapeyron vào năm 1834, và vào những năm 70 của thế kỷ 19, D. Mendeleev đã thay thế vào nó một tập hợp các giá trị không đổi của một hằng số khí phổ quát duy nhất R (8,314 J / (molK))).
Theo phương trình Clapeyron-Mendeleev, trong một hệ kín, số lượng hạt khí không đổi, do đó chỉ có ba thông số vĩ mô có thể thay đổi (T, Pvà V). Thực tế thứ hai làm nền tảng cho sự hiểu biết về các quá trình đồng thời khác nhau sẽ được thảo luận bên dưới.
Quy trình đẳng tích là gì?
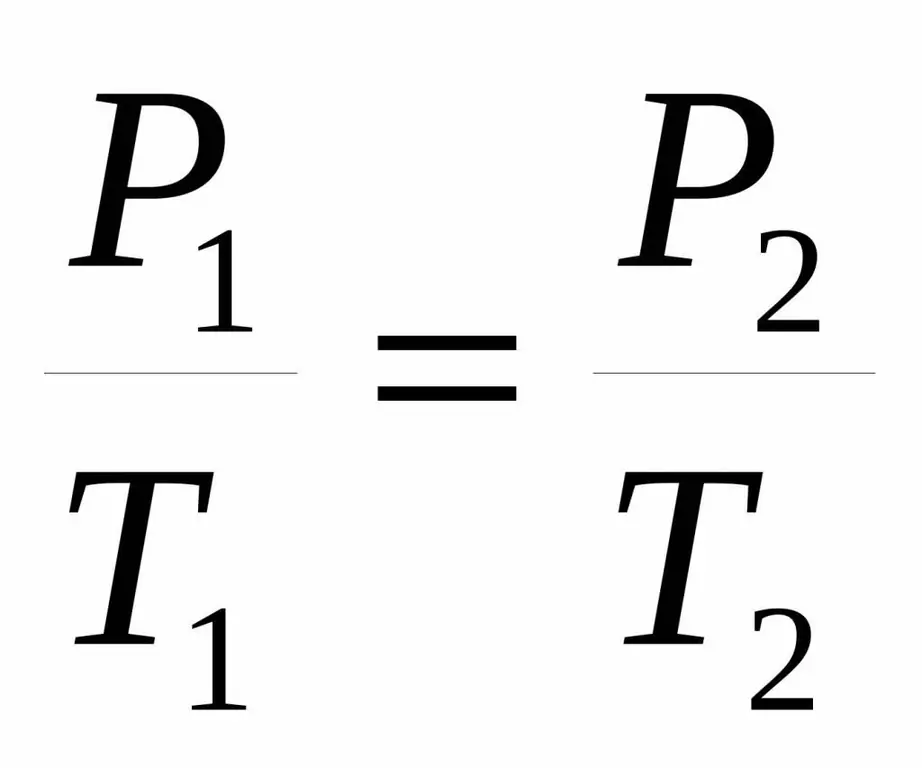
Quá trình này được hiểu là hoàn toàn bất kỳ sự thay đổi nào trong trạng thái của hệ thống, trong đó khối lượng của nó được giữ nguyên.
Nếu chúng ta chuyển sang phương trình phổ quát của trạng thái, chúng ta có thể nói rằng trong một quá trình đẳng tích chỉ có sự thay đổi áp suất và nhiệt độ tuyệt đối trong một chất khí. Để hiểu chính xác các thông số nhiệt động học thay đổi như thế nào, ta viết biểu thức toán học tương ứng:
P / T=const.
Đôi khi sự bình đẳng này được đưa ra ở một dạng hơi khác:
P1/ T1=P2/ T2.
Cả hai giá trị bằng nhau được gọi là định luật Charles theo tên của một nhà khoa học người Pháp vào cuối thế kỷ 18 đã thu được sự phụ thuộc được chú ý bằng thực nghiệm.

Nếu chúng ta xây dựng đồ thị của hàm P (T), thì chúng ta nhận được sự phụ thuộc vào đường thẳng, gọi là đường đẳng cự. Bất kỳ isochore (với mọi giá trị của n và V) là một đường thẳng.
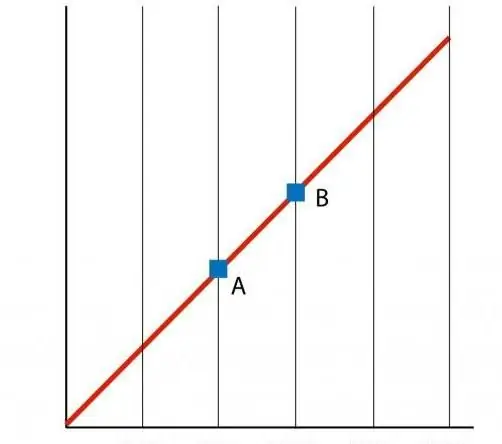
Mô tả năng lượng của quá trình
Như đã lưu ý, quá trình đẳng tích là sự thay đổi trạng thái của một hệ thống diễn ra trong một hệ thống khép kín nhưng không cô lập. Chúng ta đang nói về khả năng trao đổi nhiệt giữa chất khí và môi trường. Nói chung, bất kỳ sự cung cấp nhiệt Q nào cho hệ thống đều dẫn đến hai kết quả:
- thay đổi nội năng U;
- khíthực hiện công việc A, mở rộng hoặc ký hợp đồng.
Suy luận cuối cùng được viết theo dạng toán học như sau:
Q=U + A.
Quá trình đẳng tích của khí lý tưởng, theo định nghĩa của nó, không ngụ ý rằng khí thực hiện được công, vì thể tích của nó không thay đổi. Điều này có nghĩa là tất cả nhiệt được cung cấp cho hệ thống sẽ làm tăng năng lượng bên trong của nó:
Q=U.
Nếu chúng ta thay thế công thức rõ ràng cho nội năng vào biểu thức này, thì nhiệt của quá trình đẳng tích có thể được biểu diễn dưới dạng:
Q=z / 2nRT.
Ở đây z là số bậc tự do, được xác định bởi bản chất đa nguyên tử của các phân tử tạo nên chất khí. Đối với khí đơn nguyên, z=3, đối với khí diatomic - 5 và đối với khí triatomic và hơn thế nữa - 6. Ở đây, dưới bậc tự do, chúng ta có nghĩa là bậc tịnh tiến và độ quay.
Nếu chúng ta so sánh hiệu quả của việc đốt nóng một hệ thống khí trong quá trình đẳng tích và đẳng áp, thì trong trường hợp đầu tiên, chúng ta sẽ nhận được hiệu suất tối đa, vì trong quá trình thay đổi đẳng áp trong trạng thái của hệ thống, khí nở ra, và một phần nhiệt lượng đầu vào được sử dụng để thực hiện công việc.
Quy trình đẳng cấp
Ở trên chúng tôi đã mô tả chi tiết rằng đây là một quá trình đẳng tích. Bây giờ chúng ta hãy nói một vài từ về các isoprocesses khác. Hãy bắt đầu với isobaric. Dựa vào tên gọi, nó được hiểu là sự chuyển đổi của hệ giữa các trạng thái ở áp suất không đổi. Quá trình này được mô tả bởi định luật Gay-Lussac như sau:
V / T=const.
Giống như đường đẳng cự, thanh đẳng thế V (T) cũng biểu thị một đường thẳng trên đồ thị.
Đối vớicủa bất kỳ quá trình đẳng tích nào, sẽ thuận tiện khi tính công do khí thực hiện, vì nó bằng tích của áp suất không đổi và sự thay đổi thể tích.
Quy trình đẳng nhiệt
Đây là một quá trình trong đó nhiệt độ của hệ thống không đổi. Nó được mô tả bởi định luật Boyle-Mariotte cho một khí lý tưởng. Điều tò mò cần lưu ý rằng đây là định luật khí đầu tiên được khám phá bằng thực nghiệm (nửa sau thế kỷ 17). Ký hiệu toán học của nó trông như thế này:
PV=const.
Quá trình đẳng áp và đẳng nhiệt khác nhau về cách biểu diễn đồ thị của chúng, vì hàm P (V) là một hypebol, không phải là một mối quan hệ tuyến tính.
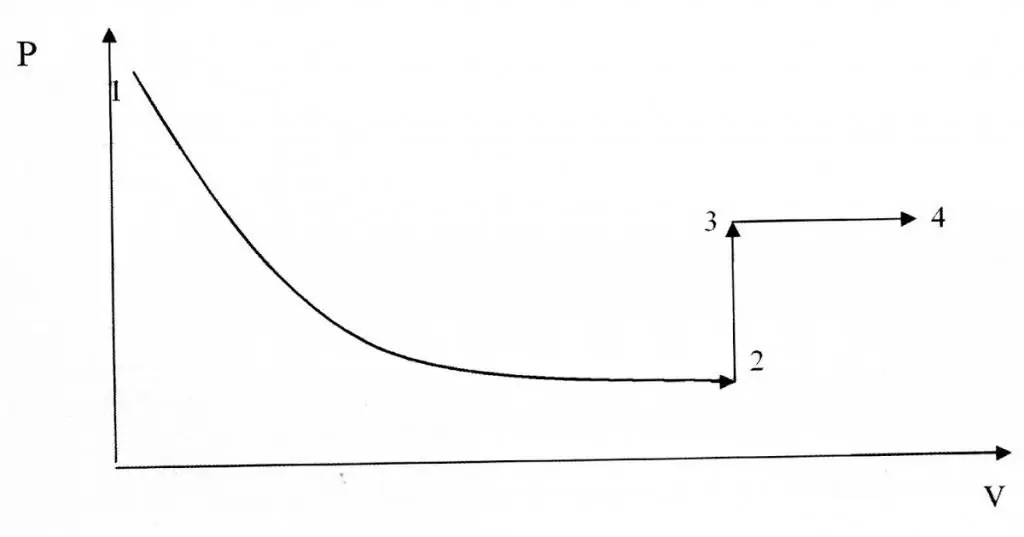
Ví dụ về giải quyết vấn đề
Hãy củng cố thông tin lý thuyết được cung cấp trong bài báo bằng ứng dụng của chúng để giải quyết một vấn đề thực tế. Biết rằng nitơ thể khí tinh khiết ở trong một xi lanh ở áp suất 1 khí và nhiệt độ 25 ° C. Sau khi nung nóng bình khí và đo áp suất trong bình thì thấy nó bằng 1,5 atm. Nhiệt độ của khí trong xilanh sau khi nung nóng là bao nhiêu? Nội năng của khí thay đổi bao nhiêu nếu trong quả bóng có 4 mol nitơ.
Để trả lời câu hỏi đầu tiên, chúng tôi sử dụng biểu thức sau:
P1/ T1=P2/ T2.
Từ nơi chúng tôi nhận được:
T2=P2/ P1 T1.
Trong biểu thức này, áp suất có thể được thay thế bằng các đơn vị tùy ýcác phép đo, vì chúng đang co lại, và nhiệt độ chỉ tính bằng kelvins. Với điều đó đã nói, chúng tôi nhận được:
T2=1.5 / 1298.15=447.224 K.
Nhiệt độ tính theo độ C là 174 ° C.
Vì phân tử nitơ là diatomic nên sự thay đổi nội năng của nó trong quá trình đốt nóng có thể được xác định như sau:
ΔU=5/2nRΔT.
Thay các giá trị đã biết vào biểu thức này, chúng ta sẽ nhận được câu trả lời cho câu hỏi thứ hai của bài toán: ΔU=+12,4 kJ.






