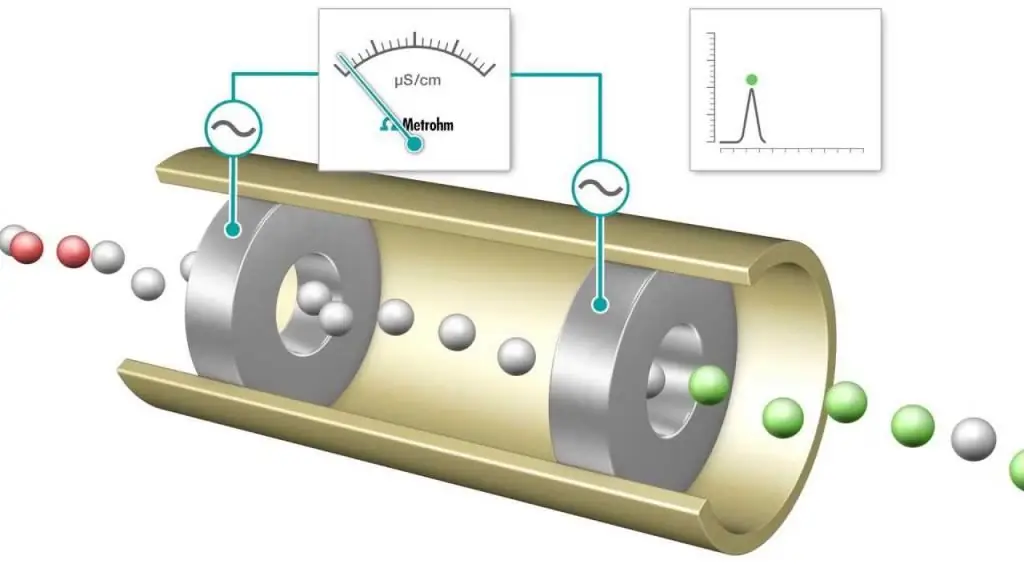
Phương pháp phân tích đo độ dẫn điện là phép đo độ dẫn điện để theo dõi tiến trình của phản ứng hóa học. Khoa học này được áp dụng rộng rãi trong hóa học phân tích, nơi chuẩn độ là một phương pháp hoạt động tiêu chuẩn. Đo độ dẫn là gì? Trong thực tế phổ biến trong hóa học phân tích, thuật ngữ này được sử dụng như một từ đồng nghĩa với chuẩn độ, trong khi nó cũng được sử dụng để mô tả các ứng dụng không chuẩn độ. Lợi ích của việc sử dụng phương pháp phân tích này là gì? Nó thường được sử dụng để xác định độ dẫn điện tổng thể của dung dịch hoặc để phân tích điểm cuối của phép chuẩn độ liên quan đến các ion.
Lịch sử
Các phép đo dẫn điện bắt đầu sớm nhất vào thế kỷ 18, khi Andreas Baumgartner nhận thấy rằng muối và nước khoáng từ Bad Gastein ởÁo dẫn điện. Vì vậy, việc sử dụng phương pháp này để xác định độ tinh khiết của nước, ngày nay thường được sử dụng để kiểm tra tính hiệu quả của hệ thống lọc nước, bắt đầu vào năm 1776. Do đó đã bắt đầu lịch sử của phương pháp phân tích đo độ dẫn.
Friedrich Kohlrausch tiếp tục phát triển ngành khoa học này vào những năm 1860, khi ông áp dụng dòng điện xoay chiều vào nước, axit và các dung dịch khác. Vào khoảng thời gian này, Willis Whitney, người đang nghiên cứu sự tương tác của axit sulfuric và phức crom sulfat, đã tìm ra điểm cuối đo độ dẫn đầu tiên. Những phát hiện này đạt đến đỉnh cao trong phép chuẩn độ điện thế và là công cụ đầu tiên để phân tích thể tích của Robert Behrend vào năm 1883 trong phép chuẩn độ clorua và bromua HgNO3. Do đó, phương pháp phân tích đo độ dẫn hiện đại dựa trên Behrend.
Sự phát triển này giúp kiểm tra khả năng hòa tan của các muối và nồng độ của các ion hydro, cũng như các phép chuẩn độ axit-bazơ và oxy hóa khử. Phương pháp phân tích đo độ dẫn đã được cải tiến với sự phát triển của điện cực thủy tinh, bắt đầu vào năm 1909.
Chuẩn độ
Chuẩn độ đo độ dẫn điện là phép đo trong đó độ dẫn điện của hỗn hợp phản ứng được theo dõi liên tục bằng cách thêm một thuốc thử. Điểm tương đương là điểm tại đó độ dẫn điện thay đổi đột ngột. Sự tăng hoặc giảm độ dẫn điện đáng chú ý có liên quan đến sự thay đổi nồng độ của hai ion dẫn điện cao nhất, ion hydro và hydroxit. Phương pháp nàycó thể được sử dụng để chuẩn độ các dung dịch có màu hoặc huyền phù đồng nhất (ví dụ: huyền phù bột gỗ) mà không thể sử dụng với các chất chỉ thị thông thường.
Chuẩn độ axit-bazơ và oxy hóa khử thường được thực hiện, sử dụng các chất chỉ thị thông thường để xác định điểm kết thúc, chẳng hạn như metyl da cam, phenolphtalein để chuẩn độ axit-bazơ và dung dịch tinh bột cho quá trình oxy hóa khử loại iot. Tuy nhiên, phép đo độ dẫn điện cũng có thể được sử dụng như một công cụ để xác định điểm cuối, ví dụ khi quan sát dung dịch HCl với bazơ mạnh NaOH.
Trung hòa proton
Khi quá trình chuẩn độ diễn ra, proton được trung hòa để tạo thành NaOH bằng cách tạo thành nước. Đối với mỗi lượng NaOH được thêm vào, một số lượng ion hydro tương đương bị loại bỏ. Trên thực tế, cation H + di động được thay thế bằng ion Na + ít di động hơn, và độ dẫn điện của dung dịch đã chuẩn độ, cũng như độ dẫn điện của tế bào đo được, giảm. Điều này tiếp tục cho đến khi đạt được điểm tương đương mà tại đó có thể thu được dung dịch natri clorua NaCl. Nếu lượng bazơ được thêm vào, lượng bazơ tăng lên khi thêm nhiều ion Na + và OH- và phản ứng trung hòa không còn loại bỏ một lượng đáng kể H +.

Do đó, khi chuẩn độ một axit mạnh bằng một bazơ mạnh, độ dẫn điện đạt cực tiểu tại điểm tương đương. Mức tối thiểu nàycó thể được sử dụng thay cho thuốc nhuộm chỉ thị để xác định điểm cuối của phép chuẩn độ. Đường cong chuẩn độ là một đồ thị của các giá trị đo được của độ dẫn điện hoặc độ dẫn điện là một hàm của thể tích dung dịch NaOH đã thêm vào. Đường cong chuẩn độ có thể được sử dụng để xác định điểm tương đương bằng đồ thị. Phương pháp phân tích đo độ dẫn (và việc sử dụng nó) cực kỳ phù hợp trong hóa học hiện đại.
Phản ứng
Đối với phản ứng giữa axit yếu với bazơ yếu, độ dẫn điện trước tiên giảm phần nào, vì một số ion H + có sẵn được sử dụng. Sau đó, độ dẫn điện tăng nhẹ lên đến thể tích của điểm tương đương do sự đóng góp của cation muối và anion (sự đóng góp này trong trường hợp gốc axit mạnh là không đáng kể và không được coi là ở đó.) Sau khi đạt đến điểm tương đương., độ dẫn điện tăng nhanh do dư thừa ion OH.
Máy dò độ dẫn điện (phương pháp phân tích đo độ dẫn điện) cũng được sử dụng để đo nồng độ chất điện phân trong dung dịch nước. Nồng độ mol của chất phân tích tạo ra độ dẫn điện của dung dịch có thể thu được từ điện trở đo được của dung dịch.
Phương pháp phân tích đo độ dẫn: nguyên tắc và công thức
(2.4.13) C=Constcell1Λm1Res, trong đó Constcell là giá trị không đổi tùy thuộc vào ô đo, Res là điện trở đo được của thiết bị (theo định luật Ohm, Res=I / V và với một hằng số đo điện áp V cường độ I cho phép bạn tính toán Res), và Λm là giá trị tương đươngđộ dẫn điện đối với các hạt ion. Mặc dù đối với các mục đích thực tế, Λm có thể được coi là không đổi, nó phụ thuộc vào nồng độ theo định luật Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, trong đó Θ là hằng số, và Λm0 là đặc trưng độ dẫn mol giới hạn của mỗi ion. Đến lượt mình, độ dẫn của mol phụ thuộc vào nhiệt độ.
Scrit
Sự phát triển của phương pháp đo độ dẫn phân tích đã đưa các nhà khoa học đến những khám phá mới. Các nhà khoa học đã xác định tỷ lệ siêu bão hòa tới hạn, Scrit, sử dụng phép đo độ dẫn trong hệ thống kết tủa AgCl đồng nhất với lượng dư ion Ag +, sử dụng thủy phân alkyl clorua làm nguồn ion CI”. Họ tìm thấy Scrit=1,51, 1,73 và 1,85 lần lượt ở 15, 25 và 35 ° C, trong đó S=([Ag +] [Cl-] / Ksp) 1/2 theo định nghĩa của họ. Nếu định nghĩa về hệ số siêu bão hòa này được chuyển đổi sang định nghĩa của chúng ta (S=[Ag +] [Cl-] / Ksp), kết quả tương ứng là 2,28, 2,99 và 3,42, tương ứng khá tốt với kết quả của nghiên cứu hiện tại. Tuy nhiên, sự phụ thuộc vào nhiệt độ của Scrit ngược lại với sự phụ thuộc vào nhiệt độ được mô tả trong nghiên cứu này. Mặc dù lý do của sự mâu thuẫn này không rõ ràng, sự giảm Scrit khi nhiệt độ tăng có thể khá hợp lý, vì tốc độ tạo mầm thay đổi đáng kể với một sự thay đổi nhỏ trong ΔGm/ kT, và do đó ΔGm/ kT, tỷ lệ với T - 3 (lnSm) 2 theo công thức (1.4.12) được coi là gần như không đổi với sự thay đổi nhiệt độ trong hệ đã cho. Ngẫu nhiên, định nghĩa của S phải là [Ag +] [Cl -] / Ksp, vì tỷ lệ siêu bão hòa vềNồng độ monome [AgCl] ban đầu được cho là S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka và Iwasaki
Lịch sử của phương pháp phân tích đo độ dẫn đã được tiếp tục bởi hai nhà khoa học nổi tiếng của Nhật Bản. Tanaka và Iwasaki đã nghiên cứu quá trình tạo mầm của các hạt AgCl và AgBr bằng phương pháp dòng dừng kết hợp với máy quang phổ đa kênh, rất hữu ích cho việc nghiên cứu một quá trình nhanh theo bậc msec. Họ nhận thấy rằng một số phức bạc halogenua cụ thể AgXm (m-1), có dải hấp thụ tia cực tím khá hẹp, được hình thành ngay lập tức khi dung dịch AgC104 có bậc 10-4 mol dm-3 được trộn với KX (X=Dung dịch Cl hoặc Br) có thứ tự từ 10-2 đến 10-1 mol dm-3, tiếp theo là sự phân rã nhanh chóng của nó trong khoảng 10 ms với sự tạo thành sản phẩm trung gian có độ hấp thụ tia cực tím rộng và sự thay đổi quang phổ chậm hơn nhiều. của sản phẩm trung gian. Họ giải thích chất trung gian là lõi đơn phân tử (AgX) n bao gồm n phân tử và xác định n từ tỷ lệ biểu kiến -dC / dt α Cn tại t=0 đối với các nồng độ ban đầu khác nhau của tiền chất C là AgXm (m-1) - (n=7 -10 đối với AgCl, n=3-4 đối với AgBr).

Tuy nhiên, vì tiền chất AgXm (m - 1) phân hủy không đứng yên, lý thuyết về sự tạo hạt nhân đứng yên không áp dụng trong quá trình này, và do đó giá trị thu được của n không tương ứng với ngiá trị của các hạt nhân tới hạn. Nếu sản phẩm trung gian chứa các hạt nhân đơn phân n,được tạo thành bởi phức đơn lượng, tỷ lệ -dC / dt α C có thể không được duy trì. Trừ khi chúng ta giả sử rằng các cụm nhỏ hơn n-m đang ở trạng thái cân bằng, ki - 1, ici - 1c1=ki, i - 1ci, với nhau trong một phản ứng tuần tự c1 → c2 → c3 →… → cn - 1 → cn., và chỉ bước cuối cùng cn - 1 → cn là không thể đảo ngược; tức là c1⇌c2⇌c3⇌… ⇌cn - 1 → cn.
Bên cạnh đó, cần giả thiết rằng nồng độ của các cụm từ 2 đến n-1 có nồng độ cân bằng không đáng kể. Tuy nhiên, dường như không có cơ sở nào để biện minh cho những giả thiết này. Mặt khác, chúng tôi đã cố gắng tính bán kính của các hạt nhân tới hạn và hệ số siêu bão hòa S ở cuối quá trình nhanh, sử dụng γ=101 mJ m - 2 đối với AgCl19 lập phương và γ=109 mJ m - 2 đối với AgBr20 lập phương, giả sử rằng các giá trị của n, 7-10 đối với AgCl19 và 3-4 đối với AgBr20, tương đương với kích thước của các hạt nhân đơn phân, n. Phương pháp đo độ dẫn phân tích, các bài đánh giá trong đó từ đơn giản là tán thành đến ngưỡng mộ, đã khai sinh ra hóa học như một ngành khoa học.
Kết quả là, các nhà khoa học đã phát hiện ra công thức sau: r=0,451 nm và S=105 cho AgCl với n=9; r=0,358 nm và S=1230 đối với AgBr với n=4. Vì hệ của họ có thể so sánh với hệ của Davis và Jones, nên hệ thống này thu được siêu bão hòa tới hạn của AgCl khoảng 1,7-2,0 ở 25 ° C. Sử dụng phép đo độ dẫn trộn trực tiếp với các thể tích bằng nhau của dung dịch nước loãng của AgNO3 và KCl, giá trị S cực cao có thể không phản ánh hệ số siêu bão hòa thực tế.ở trạng thái cân bằng với các hạt nhân trung gian.
Hấp thụ tia cực tím
Có vẻ hợp lý hơn khi gán chất trung gian có khả năng hấp thụ tia cực tím rộng cho các hạt nhân lớn hơn nhiều so với hạt nhân trung bình có phân bố kích thước rộng được tạo ra bởi phản ứng tuần tự không đứng yên. Sự thay đổi chậm chạp sau đó của các hạt nhân trung gian dường như có liên quan đến sự trưởng thành của chúng ở Ostwald.

Trong bối cảnh trên, nhà hóa học người Mỹ Nielsen cũng suy ra ntương tự khoảng 12 và S tương ứng lớn hơn 103 cho sự tạo mầm của các hạt bari sulfat từ phép đo độ đục như một hàm của siêu bão hòa, sử dụng n=dlogJ / dlogC trong một lý thuyết giống Becher-Dering cho công thức. (1.3.37), nhưng cho (n+ 1) thay vì n. Vì dung dịch của ion bari và ion sunfat được trộn trực tiếp trong thí nghiệm này, nên sự tạo mầm thoáng qua nhanh phải kết thúc ngay sau khi trộn và những gì được đo có thể là tốc độ trưởng thành Ostwald chậm sau đó và / hoặc sự hợp nhất của các hạt nhân được tạo ra. Rõ ràng, đây là lý do giải thích cho giá trị nnhỏ một cách bất hợp lý và độ bão hòa siêu cao cực kỳ cao. Do đó, một lần nữa chúng ta phải lưu ý rằng một số nguồn chứa các loài đơn phân giải phóng chúng để đáp ứng với sự tiêu thụ của chúng luôn cần thiết để đạt được sự tạo mầm gần như đứng yên trong một hệ thống kín. Tất cả các lý thuyết cổ điển về sự hình thành hạt nhân, kể cả lý thuyết Becher-Döring, đều mặc nhiên giả định một điều kiện như vậy. Định nghĩa về độ dẫnphương pháp phân tích đã được đưa ra trong các phần của bài viết trên.
Các nhà khoa học khác đã nghiên cứu quá trình tạo mầm nhất thời của bạc halogenua bằng cách phóng xạ xung của nước có chứa metylen halogenua và các ion bạc, trong đó metylen halogenua bị phân hủy để giải phóng các ion halogenua bởi các điện tử ngậm nước được tạo ra bởi bức xạ xung trong phạm vi từ 4 ns đến 3 μs. Quang phổ của các sản phẩm được ghi lại bằng cách sử dụng ống nhân quang và máy ảnh vạch và các tiền chất bạc halogenua đơn lượng được tìm thấy hình thành trong một thời gian theo thứ tự micro giây, sau đó là một quá trình tạo mầm tương tự như được quan sát bởi Tanaka và Iwasaki. Kết quả của họ cho thấy rõ ràng rằng quá trình tạo mầm bạc halogenua bằng cách trộn trực tiếp các chất phản ứng bao gồm hai bước cơ bản; nghĩa là, sự hình thành tiền chất đơn phân có bậc μs và sự chuyển tiếp sau đó thành hạt nhân bậc 10 ms. Cần lưu ý rằng kích thước trung bình của hạt nhân là khoảng 10 nm.
Bão hòa
Về hệ số siêu bão hòa cho sự tạo mầm của các hạt AgCl trong hệ thống mở, trong đó nồng độ cao của các chất phản ứng như AgNO3 và KCl liên tục được đưa vào dung dịch gelatin trong suốt quá trình kết tủa, Strong và Wey31 đã báo cáo 1,029 (80 ° C) - 1.260 (40 ° C) và Leubner32 đã báo cáo 1.024 ở 60 ° C được ước tính từ việc đo tốc độ phát triển của các hạt hạt AgCl ở độ bão hòa siêu bão hòa quan trọng. Đây là bản chất của phương pháp đo độ dẫn phân tích định lượng.
Mặt khác, đối với các hệ thống hạt AgBr mở, một sốcác giá trị ước tính của hệ số siêu bão hòa tới hạn, Scrit: Scrit∼- 1,5 ở 70 ° C theo Wey và Strong33 từ tốc độ tăng trưởng tối đa phụ thuộc vào kích thước được xác định bằng cách tìm ngưỡng tạo hạt nhân ở các tốc độ khác nhau khi thêm dung dịch AgNO3 vào KBr giải pháp với sự hiện diện của các hạt giống bởi các phản lực kép; Scrit=1,2-1,5 ở 25 ° C theo Jagannathan và Wey34 là hệ số siêu bão hòa tối đa được xác định từ phương trình Gibbs-Thomson với dữ liệu của họ về kích thước trung bình tối thiểu của các hạt nhân được quan sát bằng kính hiển vi điện tử trong bước tạo mầm của kết tủa AgBr hai tia. Điều này rất hiệu quả khi áp dụng phương pháp định lượng đo độ dẫn.

Khi tính toán các giá trị Scrit này, họ lấy γ=140 mJ m - 2. Vì sự tạo mầm trong các hệ thống mở tương ứng với quá trình tồn tại của các hạt nhân non trẻ được tạo ra trong một vùng cục bộ có độ bão hòa cực cao gần các cửa hàng chất phản ứng, rất quan trọng siêu bão hòa tương ứng với nồng độ của chất tan ở trạng thái cân bằng với các hạt nhân có kích thước cực đại, nếu chúng ta sử dụng dữ liệu của Sugimoto35 về bán kính cực đại của hạt nhân AgBr trong hệ mở (0,3 8,3 nm) với γ lý thuyết đối với AgBr khối (=109 mJ m - 2) 3, khi đó hệ số siêu bão hòa tới hạn, Scrit, được tính là 1,36 ở 25 ° C (nếu γ được giả định là 140 mJ / m2, thì Scrit=1,48).
Do đó, trong mọi trường hợp, các siêu âm quan trọng tronghệ thống mở của các hạt bạc halogenua thường thấp hơn rất nhiều so với siêu siêu âm tối đa (có thể gần với siêu siêu âm tới hạn) trong hệ thống kín. Điều này là do bán kính trung bình của các hạt nhân được tạo ra trong vùng cục bộ của một hệ mở lớn hơn nhiều so với rmtrong một hệ kín, có thể là do sự hợp nhất tức thời của các hạt nhân sơ cấp tập trung cao trong vùng cục bộ của một hệ mở với độ cao nồng độ chất điện giải cục bộ.
Đơn
Việc sử dụng phương pháp chuẩn độ đo độ dẫn để ghi liên tục trong quá trình enzym đã được nghiên cứu và phân tích rộng rãi. Hầu hết tất cả các phương pháp phân tích điện hóa đều dựa trên các phản ứng điện hóa (đo điện thế, đo điện thế, đo ampe kế, đo coul).
Phương pháp phân tích đo độ dẫn điện là một phương pháp trong đó hoặc không có phản ứng điện hóa nào trên các điện cực, hoặc có thể bỏ qua các phản ứng thứ cấp. Do đó, trong phương pháp này, tính chất quan trọng nhất của dung dịch điện phân ở lớp ranh giới là độ dẫn điện của nó, thay đổi theo một loạt các phản ứng sinh học.
Lợi ích
Cảm biến sinh học đo độ dẫn điện cũng có một số ưu điểm hơn so với các loại đầu dò khác. Đầu tiên, chúng có thể được chế tạo bằng công nghệ tiêu chuẩn màng mỏng chi phí thấp. Điều này, cùng với việc sử dụng một phương pháp tối ưu hóa để cố định vật liệu sinh học, dẫn đến giảm đáng kể chi phí chính của thiết bị vàtổng chi phí phân tích. Đối với cảm biến vi sinh tích hợp, có thể dễ dàng thực hiện chế độ đo chênh lệch, chế độ này bù đắp cho các tác động bên ngoài và cải thiện đáng kể độ chính xác của phép đo.
Dữ liệu cho thấy rõ tiềm năng to lớn của cảm biến sinh học đo độ dẫn điện. Tuy nhiên, đây vẫn là một xu hướng khá mới trong cảm biến sinh học, vì vậy việc phát triển thiết bị thương mại có một tương lai đầy hứa hẹn.
Phương pháp mới
Một số nhà khoa học đã mô tả một phương pháp chung để đo pKa bằng độ dẫn. Phương pháp này được sử dụng rộng rãi cho đến khoảng năm 1932 (trước khi các phương pháp đo pH được sử dụng). Phương pháp đo độ dẫn cực kỳ nhạy cảm với nhiệt độ và không thể được sử dụng để đo các giá trị pKa chồng lên nhau. Một lợi thế có thể có đối với các mẫu không có mang màu là nó có thể được sử dụng trong các dung dịch rất loãng, xuống đến 2,8 × 10-5 M. Trong những năm gần đây, phép đo độ dẫn 87 đã được sử dụng để đo pKa của lidocain, mặc dù kết quả thu được là 0,7 trên một đơn vị dưới giá trị pH được chấp nhận chung.

Albert và Sergeant cũng mô tả một phương pháp xác định pKa từ phép đo độ hòa tan. Như đã đề cập ở trên, độ hòa tan phụ thuộc vào pKa, vì vậy nếu độ hòa tan được đo ở nhiều giá trị pH trên một đường cong thì có thể xác định được pKa. Peck và Benet đã mô tả một phương pháp chung để ước tính giá trị pKa cho các chất đơn chất, đơn chất và lưỡng tính với một bộ các phép đo độ hòa tan và pH. Hansen và Hafliger thu được pKa của mẫu,phân hủy nhanh chóng bằng cách thủy phân từ tốc độ hòa tan ban đầu của nó như một hàm của pH trong thiết bị đĩa quay. Kết quả phù hợp với kết quả pH / UV, nhưng sự phân hủy gây khó khăn cho phương pháp sau. Nhìn chung, đây là mô tả về phương pháp phân tích đo độ dẫn.






