Kiến thức về các định nghĩa trong vật lý là yếu tố then chốt để giải quyết thành công các vấn đề vật lý khác nhau. Trong bài viết này, chúng ta sẽ xem xét ý nghĩa của các quá trình đẳng áp, đẳng áp, đẳng nhiệt và đoạn nhiệt đối với một hệ thống khí lý tưởng.
Khí lý tưởng và phương trình của nó
Trước khi tiếp tục mô tả các quá trình đẳng áp, đẳng tích và đẳng nhiệt, chúng ta hãy xem xét khí lý tưởng là gì. Theo định nghĩa này trong vật lý, họ coi một hệ thống bao gồm một số lượng lớn các hạt không thứ nguyên và không tương tác chuyển động với tốc độ cao theo mọi hướng. Trên thực tế, chúng ta đang nói về trạng thái tổng hợp của vật chất ở thể khí, trong đó khoảng cách giữa các nguyên tử và phân tử vượt xa kích thước của chúng và trong đó năng lượng tương tác của các hạt bị bỏ qua do độ nhỏ của nó, so với động năng.
Trạng thái của khí lý tưởng là tổng các thông số nhiệt động lực học của nó. Những cái chính là nhiệt độ, thể tích và áp suất. Hãy ký hiệu chúng bằng các chữ cái T, V và P, tương ứng. Vào những năm 30 của thế kỷ XIXClapeyron (một nhà khoa học người Pháp) lần đầu tiên viết ra một phương trình kết hợp các tham số nhiệt động lực học được chỉ ra trong một đẳng thức duy nhất. Nó trông giống như:
PV=nRT,
trong đó n và R lần lượt là lượng chất và hằng số chất khí.
Quá trình đẳng áp trong khí là gì?
Như nhiều người đã nhận thấy, các quá trình đẳng tích, đẳng áp và đẳng nhiệt sử dụng cùng một tiền tố "iso" trong tên của chúng. Nó có nghĩa là sự bằng nhau của một thông số nhiệt động lực học trong suốt quá trình, trong khi các thông số còn lại thay đổi. Ví dụ, một quá trình đẳng nhiệt chỉ ra rằng kết quả là nhiệt độ tuyệt đối của hệ thống được duy trì không đổi, trong khi một quá trình đẳng nhiệt biểu thị một thể tích không đổi.
Isoprocesses rất thuận tiện để nghiên cứu, vì việc cố định một trong các thông số nhiệt động lực học dẫn đến việc đơn giản hóa phương trình tổng quát của trạng thái khí. Điều quan trọng cần lưu ý là các định luật khí cho tất cả các quá trình đẳng áp này đã được khám phá bằng thực nghiệm. Phân tích của họ cho phép Clapeyron thu được phương trình phổ thông rút gọn.
Quá trình đẳng áp, đẳng tích và đẳng nhiệt
Định luật đầu tiên được phát hiện cho quá trình đẳng nhiệt trong khí lý tưởng. Bây giờ nó được gọi là định luật Boyle-Mariotte. Vì T không thay đổi nên phương trình trạng thái hàm ý đẳng thức:
PV=const.
Nói cách khác, bất kỳ sự thay đổi nào về áp suất trong hệ đều dẫn đến sự thay đổi tỷ lệ nghịch trong thể tích của nó, nếu nhiệt độ của khí được duy trì không đổi. Đồ thị của hàm số P (V) làcường điệu.
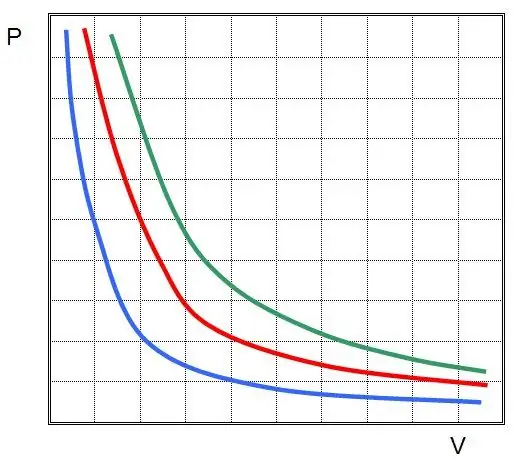
Quá trình đẳng áp - đây là sự thay đổi trạng thái của hệ thống, trong đó áp suất không đổi. Sau khi cố định giá trị của P trong phương trình Clapeyron, chúng ta thu được định luật sau:
V / T=const.
Bình đẳng này mang tên nhà vật lý người Pháp Jacques Charles, người đã nhận nó vào cuối thế kỷ 18. Thanh đẳng (biểu diễn đồ họa của hàm V (T)) trông giống như một đường thẳng. Càng nhiều áp suất trong hệ thống, đường này càng tăng nhanh.
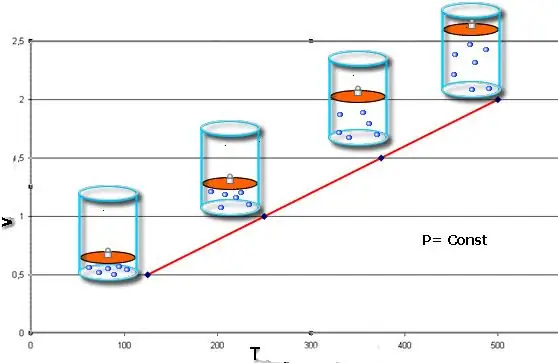
Quá trình đẳng tích rất dễ thực hiện nếu khí được đốt nóng dưới piston. Các phân tử sau cùng tăng tốc độ (động năng), tạo áp suất lớn hơn lên pít-tông, dẫn đến khí nở ra và duy trì giá trị P.
không đổi
Cuối cùng, isoprocess thứ ba là isochoric. Nó chạy với một âm lượng không đổi. Từ phương trình trạng thái, chúng ta thu được đẳng thức tương ứng:
P / T=const.
Nó được các nhà vật lý gọi là định luật Gay-Lussac. Tỷ lệ thuận giữa áp suất và nhiệt độ tuyệt đối chỉ ra rằng đồ thị của quá trình đẳng tích, giống như đồ thị của đẳng tích, là một đường thẳng có hệ số góc dương.
Điều quan trọng là phải hiểu rằng tất cả các quá trình đẳng cấp xảy ra trong các hệ thống đóng, nghĩa là giá trị của n được giữ nguyên trong quá trình của chúng.
Quy trình Adiabatic
Quá trình này không thuộc loại "iso", vì cả ba thông số nhiệt động lực học đều thay đổi trong suốt quá trình của nó. đoạn nhiệtgọi là quá trình chuyển giữa hai trạng thái của hệ, trong đó nó không trao đổi nhiệt với môi trường. Do đó, việc mở rộng hệ thống được thực hiện do dự trữ năng lượng bên trong của nó, dẫn đến giảm đáng kể áp suất và nhiệt độ tuyệt đối trong hệ thống.
Quá trình đoạn nhiệt đối với khí lý tưởng được mô tả bằng phương trình Poisson. Một trong số chúng được hiển thị bên dưới:
PVγ=const,
trong đó γ là tỷ số giữa nhiệt dung ở áp suất không đổi và ở thể tích không đổi.
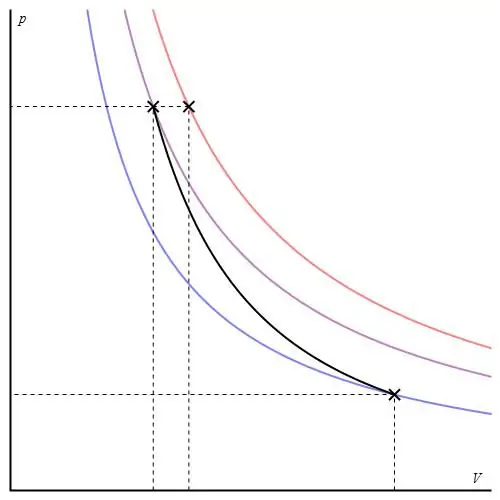
Đồ thị đoạn nhiệt khác với đồ thị quá trình đẳng tích và đồ thị đẳng tích, nhưng nó tương tự như một hyperbol (đường đẳng nhiệt). Đoạn nhiệt trong trục P-V hoạt động mạnh hơn đường đẳng nhiệt.






