Một trong những câu hỏi quan trọng trong việc nghiên cứu hệ thống nhiệt động lực học trong vật lý là câu hỏi liệu hệ thống này có thể thực hiện một số công việc hữu ích hay không. Liên quan mật thiết đến khái niệm công việc là khái niệm năng lượng bên trong. Trong bài này, chúng ta sẽ xem xét nội năng của khí lý tưởng là gì và đưa ra công thức tính nó.
Khílý
Về chất khí, là trạng thái tập hợp, không có bất kỳ lực đàn hồi nào dưới tác động bên ngoài và do đó không giữ nguyên thể tích và hình dạng, học sinh nào cũng biết. Khái niệm về khí lý tưởng đối với nhiều người vẫn còn khó hiểu và không rõ ràng. Hãy giải thích nó.
Khí lý tưởng là khí thỏa mãn hai điều kiện quan trọng sau:
- Các hạt tạo nên nó không có kích thước. Chúng có kích thước, nhưng nó quá nhỏ so với khoảng cách giữa chúng nên có thể bị bỏ qua trong tất cả các phép tính toán học.
- Các hạt không tương tác với nhau bằng lực hoặc lực van der Waalsbản chất khác. Trên thực tế, trong tất cả các khí thực đều có tương tác như vậy, nhưng năng lượng của nó không đáng kể so với năng lượng trung bình của các hạt động năng.
Các điều kiện được mô tả đều được đáp ứng bởi hầu hết các loại khí thực, nhiệt độ của chúng trên 300 K và áp suất không vượt quá một bầu khí quyển. Đối với áp suất quá cao và nhiệt độ thấp quan sát thấy sự sai lệch của các chất khí so với hành vi lý tưởng. Trong trường hợp này, người ta nói đến khí thực. Chúng được mô tả bằng phương trình van der Waals.
Khái niệm về nội năng của khí lý tưởng
Theo định nghĩa, nội năng của một hệ là tổng của động năng và thế năng chứa trong hệ này. Nếu khái niệm này được áp dụng cho khí lý tưởng, thì thành phần tiềm năng nên được loại bỏ. Thật vậy, vì các hạt của khí lý tưởng không tương tác với nhau, nên chúng có thể được coi là chuyển động tự do trong chân không tuyệt đối. Để tách một hạt khỏi hệ đang nghiên cứu, không cần thiết phải làm việc chống lại các lực tương tác bên trong, vì những lực này không tồn tại.
Như vậy, nội năng của khí lý tưởng luôn trùng với động năng của nó. Đến lượt nó, giá trị thứ hai được xác định duy nhất bởi khối lượng mol của các hạt trong hệ, số lượng của chúng, cũng như tốc độ trung bình của chuyển động tịnh tiến và chuyển động quay. Tốc độ chuyển động phụ thuộc vào nhiệt độ. Nhiệt độ tăng dẫn đến nội năng tăng và ngược lại.
Công thức chonội năng
Biểu thị nội năng của một hệ khí lý tưởng bằng chữ U. Theo nhiệt động lực học, nó được định nghĩa là hiệu giữa entanpi H của hệ với tích của áp suất và thể tích, đó là:
U=H - pV.
Trong đoạn trên, chúng ta phát hiện ra rằng giá trị của U tương ứng với tổng động năng Ekcủa tất cả các hạt khí:
Ư=Ek.
Từ cơ học thống kê, trong khuôn khổ của lý thuyết động học phân tử (MKT) của khí lý tưởng, theo đó động năng trung bình của một hạt Ek1bằng giá trị sau:
Ek1=z / 2kB T.
Ở đây kBvà T - hằng số Boltzmann và nhiệt độ, z - số bậc tự do. Tổng động năng của hệ Ekcó thể nhận được bằng cách nhân Ek1với số hạt N trong hệ:
Ek=NEk1=z / 2NkB T.
Như vậy, chúng ta đã có được công thức về nội năng của khí lý tưởng, được viết dưới dạng tổng quát dưới dạng nhiệt độ tuyệt đối và số hạt trong một hệ kín:
U=z / 2NkB T.
Khí cấu tạo và đa nguyên tử
Công thức của U được viết trong đoạn trước của bài báo không thuận tiện cho việc sử dụng thực tế, vì rất khó xác định số hạt N. Tuy nhiên, nếu chúng ta tính đến định nghĩa của lượng chất n, thì biểu thức này có thể được viết lại ở dạng thuận tiện hơn:
n=N / NA; R=NA kB=8, 314 J / (molK);
U=z / 2nRT.
Số bậc tự do z phụ thuộc vào dạng hình học của các hạt tạo nên chất khí. Do đó, đối với khí đơn nguyên tử, z=3, vì một nguyên tử chỉ có thể chuyển động độc lập theo ba hướng của không gian. Nếu chất khí là diatomic thì z=5, vì thêm hai bậc tự do quay vào ba bậc tự do tịnh tiến. Cuối cùng, đối với bất kỳ khí đa nguyên tử nào khác, z=6 (3 tịnh tiến và 3 bậc tự do quay). Với điều này, chúng ta có thể viết dưới dạng công thức sau cho nội năng của một khí lý tưởng ở dạng đơn nguyên, tảo và đa nguyên tử:
Ư1=3/2nRT;
Ư2=5/2nRT;
Ư≧ 3=3nRT.
Ví dụ về nhiệm vụ xác định nội năng
Một xi lanh 100 lít chứa hydro nguyên chất ở áp suất 3 atm. Giả sử hydro là khí lý tưởng ở những điều kiện đã cho, cần phải xác định nội năng của nó là bao nhiêu.

Các công thức trên cho U chứa lượng chất và nhiệt độ của chất khí. Trong điều kiện của bài toán, tuyệt đối không nói gì về các đại lượng này. Để giải quyết vấn đề, cần phải nhớ lại phương trình Clapeyron-Mendeleev phổ quát. Nó có hình dạng như trong hình.
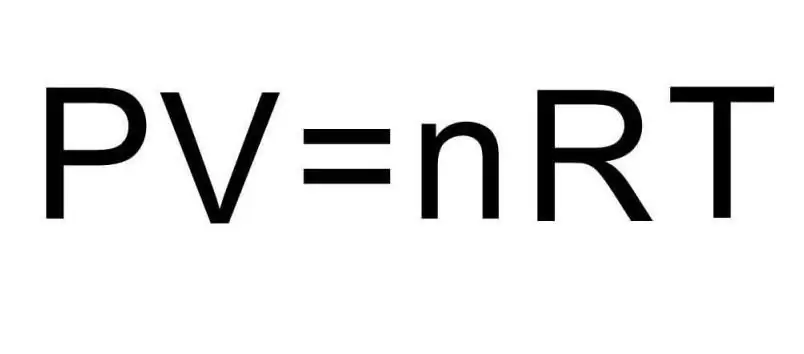
Vì hiđro H2là phân tử tảo cát nên công thức tính nội năng là:
ƯH2=5/2nRT.
So sánh cả hai biểu thức, chúng ta đi đến công thức cuối cùng để giải quyết vấn đề:
ƯH2=5/2PV.
Vẫn chuyển đổi đơn vị áp suất và thể tích từ điều kiện sang đơn vị hệ SI, thay các giá trị tương ứng trong công thức cho UH2và nhận được trả lời: UH2 ≈ 76 kJ.






